Inhaltsverzeichnis
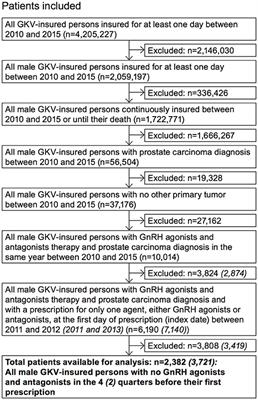
1 Einleitung
2 Medikamente zur Durchf³hrung einer Hormontherapie
3 Wann ist eine Hormontherapie anzuwenden?
4 Hitzewallungen
5 Einschrõnkungen der Sexualitõt
6 Muskelschwund und Verringerung der physischen Leistungsfõhigkeit
7 Gewichtszunahme und metabolisches Syndrom
8 Kardiovaskulõre Risiken und Diabetes
9 Verkleinerung von Hoden und Penis
10 Brustwachstum/Gynõkomastie
11 Verlust der K÷rperbehaarung
12 Gelenkschmerzen
13 Knochenschwund und -br³che, Osteoporose
14 Blutarmut/Anõmie
15 Fatigue ¢ chronische M³digkeit
16 Psychische Beschwerden
17 Kognitive Verõnderungen
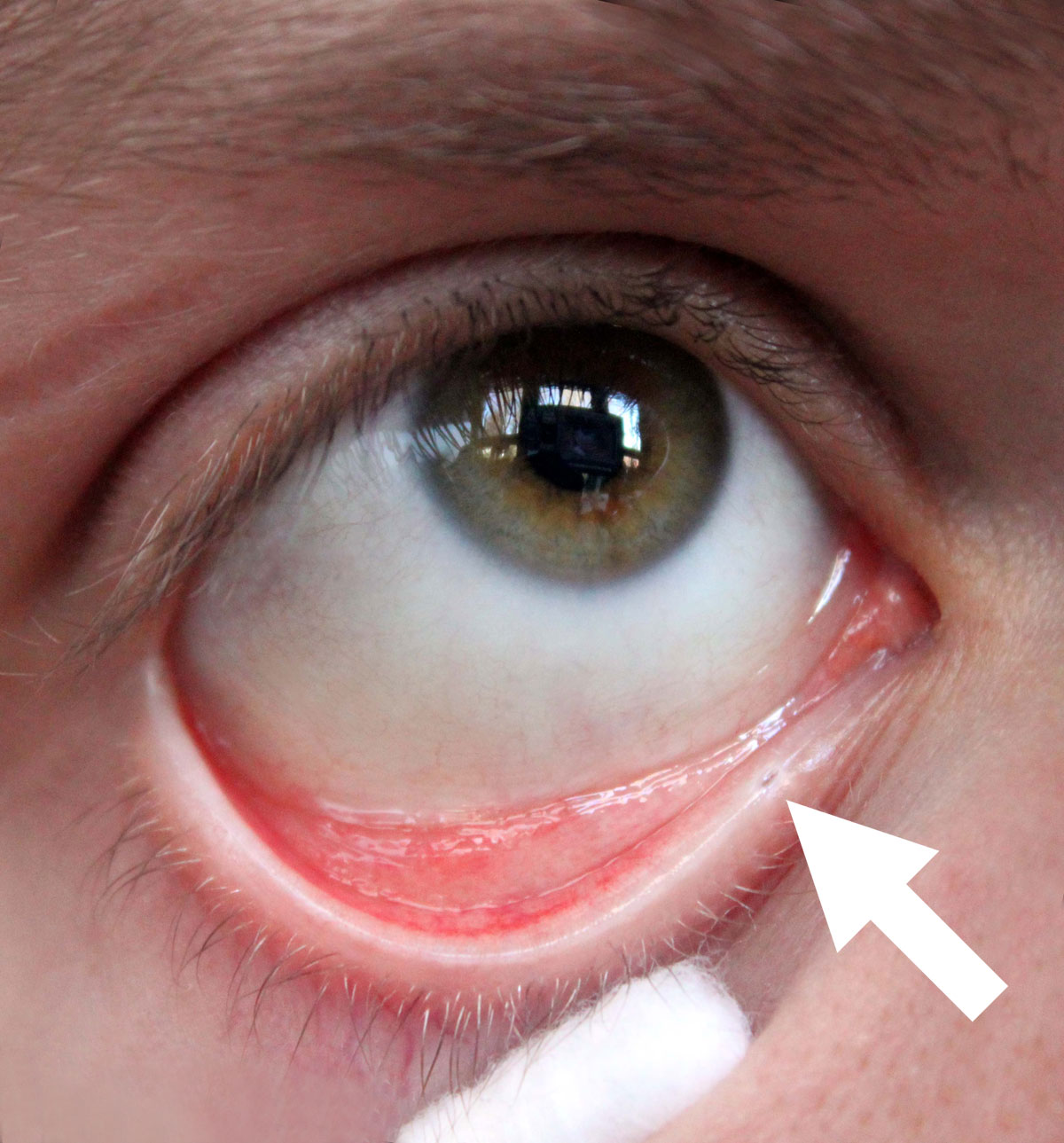
18 Trockene Augen
19 Erholung des Testosteronspiegels nach einer Hormontherapie
20 Hormontherapie mit Antiandrogenen
21 ųstrogene zur Linderung der Nebenwirkungen
22 Pharmakologie der Prõparate zur Hormontherapie
a) Zellbiologische Grundlagen
b) Orchiektomie
c) GnRH Analoga
d) GnRH Antagonisten
e) Antiandrogene
f) Hemmer der Testosteron-Biosynthese
g) Neue Androgenrezeptorhemmer
h) ųstrogene
23 Schlu▀betrachtung
24 Quellenverzeichnis
1 Einleitung
Die Hormontherapie ist eine sehr effektive Therapie gegen das Wachstum des Prostatakrebses. Fast alle Patienten, die nicht durch eine Operation oder Bestrahlung den Tumor beseitigen konnten, m³ssen irgendwann eine Hormontherapie machen. Diese Therapie wird dann f³r die verbleibende Lebenszeit angewendet. Oft wird auch bei einer Bestrahlung eine Hormontherapie von zwei bis drei Jahren durchgef³hrt.
Eine Hormontherapie ist mit vielen Nebenwirkungen verbunden. Diese treten nicht alle bei jedem Patienten auf und in der Regel auch mit individuell unterschiedlicher Intensitõt. An manche Nebenwirkungen gew÷hnen sich die Patienten auch und manche belasten dessen soziales Umfeld mehr als den Patienten selbst.
Der Arzt wird empfehlen, mit einer Hormontherapie zu beginnen, wenn er dies aus Sicht der Krebsbekõmpfung f³r richtig erachtet. Viele ─rzte sprechen mit dem Patienten nicht ³ber Nebenwirkungen. Sollte der Arzt ihm alle Nebenwirkungen eingehend erlõutern, w³rden die meisten Patienten gro▀e Bedenken haben mit einer Hormontherapie zu beginnen. Viele Patienten sprechen spõter die Nebenwirkungen beim Arzt nicht an oder wissen auch nicht, dass diese durch die Hormontherapie verursacht werden. Manche ─rzte bestõtigen dann nur, dass es sich um eine bekannte Nebenwirkung handelt. Der Arzt konzentriert sich auf die Wirkung der Hormontherapie, die durch die Entwicklung des PSA Wertes verfolgt wird und wird dem Patienten oft keine Empfehlungen geben, wie dieser mit den Nebenwirkungen umgehen kann. Entsprechend erwõhnt der Beipackzettel der eingesetzten Medikamente nur welche Nebenwirkungen auftreten k÷nnen, aber nicht, was der Patient dagegen tun k÷nnte. Da die Hormontherapie ³ber viele Jahre angewendet wird, kann dies zu einer gro▀e Belastung f³r den Patienten f³hren.
Wenn ein neues Medikament zugelassen werden soll, so bedarf dies gro▀er und teurer Studien, sogenannter Phase III Studien. In Bezug auf die Nebenwirkungen der Medikamente f³r eine Hormontherapie liegen keine entsprechenden, gro▀en Studien vor. Daher basieren die in dieser Arbeit verwendeten Studien auf kleineren Teilnehmerzahlen und haben daher nicht die hohe Evidenzkategorie wie gro▀e Phase III Studien. Dies muss man bei der Bewertung der Studienergebnisse ber³cksichtigen. Diese Studien liefern keine endg³ltigen Beweise, sind aber deutlich hilfreicher als keine Studien. Manchmal liegen auch Studien mit widersprechenden Ergebnissen vor. Im Rahmen dieser Arbeit konnte aber keine vergleichende Bewertung dieser Studien durchgef³hrt werden.
Es wird im folgenden ein ▄berblick ³ber die verschiedenen Nebenwirkungen gegeben, die bei einer Hormontherapie auftreten k÷nnen und die M÷glichkeiten zur Linderung oder Vermeidung dieser Nebenwirkungen aufgezeigt. Ziel ist es den betroffenen Patienten, die eine Hormontherapie machen m³ssen, damit zu helfen.
2 Medikamente zur Durchf³hrung einer Hormontherapie
Eine Hormontherapie kann mit verschiedenen Medikamenten durchgef³hrt werden. Fast immer sind dies sogenannte GnRH-Analoga (Leuprorelin, Goserelin, Triptorelin oder Buserelin) oder GnRH-Antagonisten (z.B. Degarelix). Au▀erdem k÷nnen die Hoden operativ entfernt werden, das ist die sogenannte Orchiektomie. Man bezeichnet die Hormontherapie auch als ADT, diese Abk³rzung steht f³r Androgendeprivationstherapie oder Androgenentzugstherapie. In dieser Arbeit wird die Androgenentzugstherapie mit GnRH-Analoga, GnRH-Antagonisten oder Orchiektomie als ADT bezeichnet und es werden die von diesen Mitteln verursachten Nebenwirkungen behandelt. Daneben gibt es noch Antiandrogene, vor allem Bicalutamid, die andere Nebenwirkungen zeigen und daher in einem gesonderten Kapitel behandelt werden. Die Therapie mit Antiandrogenen wird in diesem Text nicht als ADT bezeichnet. Wird dagegen von Hormontherapie gesprochen, so ist beides, eine ADT und eine Therapie mit Antiandrogenen gemeint.
Die Prostatakrebszellen besitzen Androgen-Rezeptoren die das Testosteron im K÷rper eines Mannes binden. Dieses Testosteron ben÷tigt die Tumorzelle f³r ihr weiteres Wachstum. Wenn man den Testosteronspiegel im K÷rper durch eine ADT senkt, so k÷nnen die Tumorzellen kein Testosteron aufnehmen und das Wachstum dieser Zellen wird gestoppt. Manche Zellen sterben dadurch auch ab. Andere Tumorzellen sind jedoch resistent und wachsen trotzdem weiter, auch ohne oder mit nur sehr wenig Testosteron.
Eine ADT wird heute weit ³berwiegend medikament÷s durchgef³hrt, das operative Entfernen der Hoden, die Orchiektomie, wird nur noch selten angewandt. Man kann diese Operation nicht mehr r³ckgõngig machen, wenn starke Nebenwirkungen auftreten sollten. Es sei denn, man f³hrt das Testosteron durch Medikamente wieder zu.
Am hõufigsten werden GnRH-Agonisten eingesetzt. Dies sind Spritzen, die es in Ein-, Drei oder Sechs-Monats-Depots gibt. Diese GnRH-Agonisten gibt es in verschiedenen Wirkstoffen, die unter verschiedenen Handelsnamen angeboten werden:
Leuprorelin (Enantone«, Trenantone«, Eligard«)
Goserelin (Zoladex«)
Triptorelin (Decapeptyl«, Pamorelin«)
Buserelin (Profact«, Metrelef«, Suprecor«, Suprefact«)
Am bekanntesten ist der Wirkstoff Leuprorelin. Davon enthõlt Eligard« doppelt so viel wie die anderen beiden Medikamente Enantone« und Trenantone«.
Daneben gibt es GnRH-Antagonisten, von denen derzeit nur Firmagon« mit dem Wirkstoff Degarelix eine praktische Bedeutung hat.
Die im folgenden betrachteten Nebenwirkungen werden durch Orchiektomie, GnRH-Analoga und GnRH-Antagonisten verursacht. Diese Mittel senken den Testosteronspiegel im K÷rper ab. Es gibt daneben auch Antiandrogene, die als Tabletten eingenommen werden und eine ganz andere Wirkungsweise haben, so dass diese Nebenwirkungen nicht oder in erheblich geringerem Umfang auftreten. Die ─rzte gehen allgemein davon aus, dass diese Antiandrogene keine so effektive Wirkung gegen den Tumor haben wie die erwõhnten GnRH-Agonisten und GnRH-Antagonisten.
3 Wann ist eine Hormontherapie anzuwenden?
Die Nebenwirkungen eine ADT lassen sich nat³rlich am einfachsten vermeiden, in dem keine Hormontherapie durchgef³hrt wird. Man sollte daher jeweils genau pr³fen, ob wirklich eine Hormontherapie in der aktuellen Situation erforderlich ist. Es gibt verschiedene Krankheitsituationen, in denen eine Hormontherapie eingesetzt wird. Diese sind:
a) Umfangreiche Metastasen werden bereits bei der Diagnose festgestellt
In diesem Fall gehen die Leitlinien davon aus, dass der Krankheitsverlauf durch eine Operation oder Bestrahlung nicht mehr kurativ behandelt werden kann und empfehlen mit einer Hormontherapie zu beginnen. Diese wird dann lebenslang fortgef³hrt. Neuere Studien zeigen allerdings, dass der Krankheitsverlauf auch in dieser Situation durch eine Operation oder Bestrahlung positiv beeinflusst werden kann (Choudhury 2019)(Parker 2018)(Knipper 2019). Auf die Hormontherapie kann in diesem Fall aber trotzdem nicht verzichtet werden.
b) Als begleitende Therapie bei einer Bestrahlung
Wenn sich der Patient, meist bei fortgeschrittenem Alter, f³r eine Strahlentherapie der Prostata entscheidet, so zeigen Studien, dass der Erfolg dieser Strahlentherapie deutlich verbessert wird, wenn gleichzeitig mit einer ADT begonnen wird. Teilweise wird damit auch schon vor der Bestrahlung begonnen. Umstritten ist, wie lange die ADT in diesem Fall durchzuf³hren ist. Die grundlegende Studie dazu (Bolla 2009) empfiehlt eine Dauer von 36 Monaten, also drei Jahre. In dieser Studie wurde auch festgestellt, dass sechs Monate ADT keine entsprechende Wirkung hatten. Eine ADT ³ber drei Jahre ist f³r einen Patienten eine erhebliche Belastung und manche der eingetretenen Nebenwirkungen, wie erektile Dysfunktion, bilden sich oft nach dem Ende der ADT nicht mehr zur³ck. Kritiker dieser Studie wenden ein, dass zum Zeitpunkt dieser Studie mit niedrigeren Strahlendosen als heute gearbeitet wurde und daher jetzt m÷glicherweise eine k³rzere Dauer der begleitenden ADT m÷glich sei. Es gibt jetzt eine neuere, Phase-III Studie (Nabid 2018), die feststellte, dass 18 Monate begleitende ADT die gleiche Wirkung wie eine ADT ³ber 36 Monate hat. Bei neueren Bestrahlungstechniken, die mit h÷heren Strahlendosen arbeiten wie die SBRT Bestrahlung, konnte kein Vorteil f³r eine begleitende ADT festgestellt werden. Auch bei der Brachytherapie zeigte sich ein lõngeres ▄berleben bei nur 6 Monaten ADT gegen³ber einer lõngeren ADT (Stone 2018).
c) Als begleitende Therapie bei einer Salvage-Bestrahlung
Wenn nach einer Prostata-Operation der PSA Wert ansteigt, so wird oft eine Bestrahlung der Prostata durchgef³hrt, um dort m÷glicherweise vorhandene Tumorreste zu beseitigen. In diesem Fall sehen die Leitlinien keine begleitende Hormontherapie vor. In Studien wurde jedoch eine begleitende ADT von sechs Monaten (Carrie 2019) oder eine Hormontherapie mit Bicalutamid von 24 Monaten (Shipley 2017) mit gutem Erfolg durchgef³hrt. Vor allem bei Patienten mit h÷herem Risiko kann daher eine entsprechende Hormontherapie sinnvoll sein. Die Studie von Shipley wurde vor kurzem neu ausgewertet (Spratt 2019). Dabei wurde deutlich, dass die begleitende Hormontherapie nur bei Patienten mit hohem Risiko einen Vorteil zeigte. Als Patienten mit hohem Risiko wurden Betroffene mit eine PSA Wert von gr÷▀er 1,5 ng/ml vor Beginn der Bestrahlung eingestuft.
d) Bei einem biochemischen Rezidiv
In vielen Fõllen steigt nach einer Bestrahlung oder einer Salvage-Bestrahlung nach Operation der PSA Wert wieder an. In der Regel ist der Betroffene und sein soziales Umfeld dar³ber sehr besorgt. Die ³berwiegende Mehrheit der Urologen wird daraufhin mit einer ADT beginnen. Der PSA Wert fõllt daraufhin stark, der Patient ist zufrieden und der Arzt ebenfalls. Die Frage ist allerdings, ob angesichts der Nebenwirkungen einer ADT dieses Vorgehen in dieser Situation sinnvoll ist. Vorliegende Studien konnten durch eine Senkung des PSA Wertes kein lõngeres ▄berleben nachweisen. Zwei kleinere Studien (Messing 2006)(Duchesne 2016, TOAD Studie) k÷nnen auf Grund viel zu niedriger Teilnehmerzahlen keine validen Aussagen dazu machen. So zeigte eine gemeinsame Auswertung der TOAD und der ELAAT Studien keinen Vorteil f³r einen fr³hen Beginn der ADT (Loblaw 2018). Die Leitlinien empfehlen daher, den Anstieg des PSA Wertes nicht mit einer ADT zu bekõmpfen. Diese Empfehlung der Leitline bleibt jedoch weitgehend unbeachtet. So wurde in einer deutschen Studie festgestellt, dass 70% der Patienten, die mit einer ADT begannen, noch keine Metastasen zeigten (Hupe 2018).
Die Leitlinie erwõhnt, man solle bei einem steigenden PSA Wert in dieser Situation mit einer Hormontherapie beginnen bei (Leitlinie Prostatakarzinom, Erlõuterung zu Punkt 6.16):
Ģ einer PSA-Verdopplungszeit < 3 Monate;
Ģ symptomatischer lokaler Progression;
Ģ nachgewiesener Fernmetastasierung.
Man geht wohl davon aus, dass bei einer PSA-Verdopplungszeit kleiner als drei Monaten von vorhandenen Metastasen auszugehen ist. Unter symptomatischer lokaler Progression ist das Auftreten von Schmerzen durch Metastasen gemeint, mit Fernmetastasierung Metastasen au▀erhalb des Beckenbereichs. Diese Metastasen sollten aber mit einem CT oder Knochenszintigramm festgestellt werden und nicht mit einem PSMA PET/CT, das viel fr³her als die von der Leitlinie zugrunde gelegten Studien Metastasen nachweisen kann.
Wenn der Betroffene von dem PSA Anstieg sehr beunruhigt ist, kann man auch eine intermittierende Hormontherapie mit Bicalutamid durchf³hren, um den PSA Wert zu senken. Dieses Mittel hat nur geringe Nebenwirkungen und kann im sechsmonatigen Wechsel eingesetzt werden. Wenn Bicalutamid keine Wirkung mehr hat, k÷nnen ein GnRH-Analogon oder andere Medikamente wie Flutamid eingesetzt werden.
e) Hormontherapie nach einer Operation
Bei anderen Tumorarten, z.B. Darmkrebs, wird nach der Operation eine Chemotherapie durchgef³hrt, um verbliebene Tumorzellen dadurch abzut÷ten. Damit vergleichbar kann man auch nach einer Prostata-Operation eine sechsmonatige ADT durchf³hren. Wie in einer gro▀en Studie gezeigt wurde, f³hrt dies auch bei Patienten mit hohem Risiko zu einem sehr guten Krankheitsverlauf ³ber zehn Jahre nach der Operation (Dorff 2011, Hussain 2018a).
4 Hitzewallungen
Die ADT senkt den Testosteronspiegel und in der Folge davon den ųstrogenspiegel. Das Senken des ųstrogenspiegels bewirkt beim Mann Hitzewallungen wie sie auch von Frauen in den Wechseljahren bekannt sind (Russell 2017)(Taylor 2016). Diese Hitzewallungen treten bei etwa 60% der Mõnner wõhrend einer ADT auf (Walker 2013). Sie f³hren zu Schwindel, Herzklopfen und ausgeprõgten Schlafst÷rungen. Allein diese an sich harmlose Nebenwirkung veranlasst einen gro▀en Teil der Patienten die ADT abzubrechen (Allan 2014).

(Bild aus Frydenberg 2019)
Das abgesenkte ųstrogen senkt den Temperatursollwert im prõoptischen Bereich des vorderen Hypothalamus (Allan 2014). Die ─nderungen der Temperatur der Haut wird von spezialisierten Nervenzellen registriert und an das R³ckenmark gemeldet. Die Signale werden von dort aus ins Stammhirn weitergeleitet, und zwar an die Nervenzellen in einer Stammhirnregion namens Nukleus parabrachialis. Dies aktiviert wiederum die erwõhnte prõoptische Region (Nakamura 2008). Wurde dort der Temperatursollwert durch den ųstrogenmangel gesenkt, so beginnt man zu schwitzen obwohl die Au▀entemperatur dies nicht erforderlich machen w³rde. Dieser Temperatursollwert ist nun individuell unterschiedlich stark gest÷rt, so dass die Patienten unterschiedlich starke Beschwerden haben.
Bei Patienten, die diese Zusammenhõnge kennen, l÷sen diese Beschwerden keine Besorgnis aus. Luftdurchlõssige Kleidung aus Baumwolle, niedrige Temperaturen im Schlafzimmer und die Vermeidung bekannter Faktoren, die eine Hitzewallung ausl÷sen k÷nnen, erm÷glichen den Patienten diese Beschwerden zu bewõltigen. Als solche Faktoren werden genannt: erh÷hte Umgebungstemperaturen, Stress, Angstzustõnde, scharfe Lebensmittel, Kaffee und Alkohol. Als Hausmittel gegen Hitzewallungen wird auch Salbeitee empfohlen (Janzer 2009). Als Alternative zu Salbeitee gibt es auch Tabletten mit Salbeiblõtter-Trockenextrakt, die unter dem Namen Sweatosan angebotenen werden.
Frauen und teilweise auch Mõnner verwenden pflanzliche Mittel gegen Hitzewallungen. Dies sind die Wirkstoffe der Traubensilberkerze, die unter dem Namen Remifen und Remifen plus angeboten werden. Au▀erdem sibirischer Rhabarber, der unter dem Namen femiLoges im Handel ist. Dar³ber hinaus gibt es diverse Kombinationsprõparate mit verschiedenen weiteren Pflanzenstoffen. Man bezeichnet diese teilweise als Phyto÷strogene, da sie eine strukturelle ─hnlichkeit mit den ųstrogenen besitzen. Diese ─hnlichkeit erm÷glicht offenbar eine Bindung an ųstrogenrezeptoren.
Es gibt weitere M÷glichkeiten, diese Hitzewallungen zu bekõmpfen. Bei Frauen wird eine ųstrogen-Ersatztherapie mit ųstradiol-Pflastern angeboten. Da die Hitzewallungen auch beim Mann durch einen niedrigen ųstrogenspiegel verursacht werden, wirken diese Pflaster auch bei Mõnnern (Gerber 2000).
Man kann auch Medikamente nehmen, die allerdings mit Nebenwirkungen verbunden sind. So k÷nnen Antidepressiva der SNRI oder SSRI Klassen wie Gabapentin(Neurontin«) und Venlafaxin(Effexor«) oder auch Clonidin eingesetzt werden (Barbieri 2013) (Laufer 1982) (Loprinzi 1994) (Loprinzi 2009) (Boekhout 2008). Au▀erdem lassen sich Cyproteronacetat(Androcur«) oder eine Spritze Medroxyprogesteronacetat(MPA) (Provesa«) gegen Hitzewallungen einsetzen (Irani 2009).
Die Prostatakrebsleitlinie erwõhnt zur Linderung von Hitzewallungen Cyproteronacetat ä in einer Dosierung von 50 mg 2 x 1 Tbl. oder 300 mg i.m. alle zwei Wochenō. Au▀erdem werden ųstrogene und Progesteron sowie Clonidin oder Antidepressiva erwõhnt. (Leitlinie Prostatakarzinom, Erlõuterung zu Punkt 6.16)
Schlie▀lich kann auch Akupunktur eingesetzt werden, um die Hitzewallungen zu reduzieren (Beer 2010)(Frisk 2014). Damit konnten bei 41% der Patienten die Hitzewallungen um mehr als 50 % reduziert werden (Beer 2010). Empfohlen wird eine Behandlung zweimal die Woche wõhrend der ersten vier Wochen, danach einmal die Woche f³r sechs weitere Wochen. Folgende Punkte sollen dabei genadelt werden:
bilateral: Gallenblasen Gb 34, Blasen Bl 15, Bl 23, Bl 32,
unilateral: Dumai GV/Du 20, Herz He 7, Kreislauf Ks 6, Leber Le 2 und Milz Mi 6.
Die Punkte Bl 23 und Bl 32 erhalten eine Niedrig-Frequenz Elektrostimulation (2 Hz)
(Beer 2010). Die angegebenen Organe beziehen sich auf die Mediane, auf denen die Punkte liegen.
Bei all diesen Mitteln muss man ber³cksichtigen, dass ein Placebo bei etwa 25% der Patienten zu einer Besserung der Hitzewallungen um ³ber 50% f³hrt (Kaplan 2014). Dies entsprach in einer Studie der Wirkung von niedrig dosiertem Gabapentin (Loprinzi 2009).
5 Einschrõnkungen der Sexualitõt
Durch die ADT kommt es bei fast allen Patienten zu Erektionsst÷rungen, also einer erektilen Dysfunktion. Das hei▀t, es ist keine Erektion des Penis mehr m÷glich.

(Bild aus van Oort 2019)
Vielfach ist zusõtzlich die Potenz der Patienten bereits vor Beginn der ADT altersbedingt oder durch eine Operation oder Bestrahlung geschwõcht. Ebenfalls schwõcht die Gewichtszunahme wõhrend einer ADT die Potenz (Hatzimouratidis 2007). Dar³ber hinaus lõsst die Libido, also das Interesse an Sexualitõt, durch die ADT stark nach. Diese Nebenwirkungen m³ssen auch mit der Partnerin des Patienten besprochen werden, da die Partnerschaft davon sehr beeintrõchtigt werden kann. ▄ber 80% der Patienten stellen ihre sexuellen Aktivitõten wõhrend einer ADT ein (Walker 2013).
Jeder Mann hat nachts, meist unbemerkt, Erektionen. Diese finden nach Beginn der ADT auf Grund der Absenkung des Testosterons nicht mehr statt. Durch die mangelnde Libido reduziert der Patient ebenfalls die Zahl der Erektionen. Dies f³hrt nach ungefõhr sechs Monaten zu einer Penisatropie, die Schwellk÷rper schrumpfen und eine Erektion ist nicht mehr m÷glich, da das Abflie▀en des Blutes aus den Schwellk÷rpern nicht mehr verhindert werden kann (Aoun 2015). Diese Penisatropie beginnt sich schon nach einigen Wochen zu entwickeln. Daher sind ein gro▀er Teil der Patienten auch nach dem Ende der ADT dauerhaft impotent. Dem kann nur entgegengewirkt werden, wenn der Patient trotz mangelnder Libido regelmõ▀ig f³r Erektionen sorgt! Eine Impotenz nach dem Ende der ADT wird in vielen Fõllen die Partnerschaft weiter belasten. Sie hat oft gravierende Auswirkungen auf die Psyche. Es kann zur Vereinsamung aufgrund von Scham, auf eine Einstellung sexueller Aktivitõten und einem Verlust des Selbstwertgef³hls kommen.
Ein Mann kann auch ohne Erektion durch entsprechende Stimulation einen Orgasmus haben. Auch die Frau ben÷tigt keine Penetration, um zu einem Orgasmus zu kommen. Viele Paare haben daher gemeinsamen Sex in dem sie sich entsprechend darauf eingestellt haben. Dar³ber hinaus lõsst sich eine erektile Dysfunktion durch Medikamente, die die Erektion verstõrken oder andere Ma▀nahmen teilweise beheben. Geeignete Medikamente sind z.B. Sildenafil (Viagra«) oder Tadalafil (Cialis«), die mittlerweile als Generika verf³gbar sind. Der Testosteron-Entzug wõhrend einer ADT soll allerdings die Wirkung dieser Medikamente reduzieren (White 2015) (Alhathal 2012). Dies gilt insbesondere wenn bereits eine Penisatropie eingetreten ist.
Alternativ gibt es auch den Wirkstoff Alprostadil, der vom Patienten selbst injiziert werden muss. Dieser ist auch dann wirksam, wenn die Erektionsst÷rungen durch eine Schõdigung der Nerven im Rahmen einer Prostataoperation hervorgerufen wurden. Dieser Wirkstoff kann als Fertigspritze, Harnr÷hrenstõbchen (MUSE«) oder Gel verabreicht werden. Die Spritze hat etwa die Gr÷▀e einer Insulinspritze und damit wird das Mittel direkt in den Schwellk÷rper des Penis injiziert. Man nennt dies auch eine Schwellk÷rper-Autoinjektions-Therapie (SKAT). Das Gel wird dagegen mit einem Applikator in die Harnr÷hre gedr³ckt. Die erste Anwendung und Einweisung erfolgt in der Regel durch den Urologen, der erst danach ein Rezept ausstellen sollte.
Eine Erektion lõsst sich auch mit einer Vakuumpumpe herbeif³hren. Anschlie▀end wird ein Gummiring ³ber die Penisbasis gest³lpt, der das Abflie▀en des Blutes verhindert. Nach einiger ▄bung ist das erfolgreich einsetzbar.
Schlie▀lich gibt es noch Schwellk÷rperprothesen, die im Rahmen einer Operation in den Penis implantiert werden. Diese Operation kann recht schmerzhaft sein. Alle diese Mittel setzen allerdings voraus, dass trotz ADT ausreichend Libido f³r sexuelle Aktivitõten verblieben ist.
6 Muskelschwund und Verringerung der physischen Leistungsfõhigkeit
Durch das Absenken des Testosteronspiegels kommt es zu einer Reduktion der Muskelmasse (Sarkopenie). Nach 12 Monaten sind beispielsweise einer Studie von Smith zufolge im Mittel 3,8 % der Muskelmasse zur³ckgegangen (Smith 2004). Dies f³hrt zu einer verminderten Leistungsfõhigkeit, die sich bei den Patienten meist deutlich bemerkbar macht (Storer 2012). Treppensteigen, bergauf gehen usw. fõllt deutlich schwerer. Im Bodybuilding Bereich wird oft Testosteron zugef³hrt, um die Muskelmasse zu erh÷hen. Entsprechend vermindert sich die Muskelmasse, wenn das Testosteron durch eine ADT gesenkt wird.
Dem Muskelschwund kann nur durch regelmõ▀iges Krafttraining entgegengewirkt werden (GalvŃo 2006). Frauen, k÷nnen trotz niedrigem Testosteronspiegel durch Krafttraining Muskeln aufbauen. Krafttraining bedeutet Gewichtheben, Kniebeugen, Klimmz³ge, Liegest³tzen oder ▄bungen an entsprechenden Gerõten, die am besten in einem Fitnesszentrum unter Anleitung eines Trainers durchgef³hrt werden. Krafttraining verbessert das Befinden der Patienten deutlich (Segal 2003).
7 Gewichtszunahme und metabolisches Syndrom
Nach dem Beginn der ADT tritt bei den meisten Patienten eine Gewichtszunahme ein. Diese ist nicht durch die Testosteronabsenkung sondern durch die resultierende ųstrogenabsenkung bedingt (Finkelstein 2013).

(Bild aus Meerleer 2016)
Die Gewichtszunahme betrõgt im Mittel 1,8%, dies sind bei einem Gewicht von 90 kg also 1,6 kg. Wie bereits erwõhnt, geht jedoch die Muskelmasse zur³ck (sarcopenic obesity). Der dadurch bedingte Gewichtsverlust wird durch einen Zuwachs an K÷rperfett ³berkompensiert. Das K÷rperfett erh÷ht sich um 11%, also ganz erheblich (Smith 2004). Andere Studien berichten von unterschiedlichen Werten. Der Zuwachs an K÷rperfett erh÷ht die kardiovaskulõren Risiken und kann zu einem metabolischen Syndrom f³hren (Smith 2001a). Die Symptome f³r ein metabolische Syndrom beginnen sich bereits innerhalb von 12 bis 24 Wochen nach Beginn der ADT zu entwickeln (žstergren 2018)(Mitzuzuka 2016).
Unter dem Begriff äMetabolisches Syndromō werden verschiedene Krankheiten und Risikofaktoren f³r Herz-/Kreislauferkrankungen zusammengefasst, die sich in der Regel durch eine ▄berernõhrung entwickeln. Folgende Symptome bzw. Krankheitsbilder treten beim Metabolischen Syndrom meist gemeinsam auf (Nguyen 2015):
Ģ starkes ▄bergewicht mit meist bauchbetonter Fetteinlagerung (Adipositas)
Ģ Bluthochdruck
Ģ erh÷hter Blutzuckerspiegel (gest÷rter Zuckerstoffwechsel in Form einer
Ģ Insulinunempfindlichkeit bzw. -Resistenz), eine Hauptursache f³r Diabetes
Ģ gest÷rter Fettstoffwechsel, Hypertriglyzeridõmie und erniedrigtes HDL-Cholesterin
Das metabolische Syndrom wird neben dem Rauchen als der entscheidende Risikofaktor f³r Erkrankungen der arteriellen Gefõ▀e, insbesondere die koronare Herzkrankheit, angesehen. Mõnner mit einem metabolischen Syndrom sterben doppelt so hõufig an einem Herzinfarkt oder Schlaganfall wie gesunde Mõnner. Das Risiko eine Diabetes mellitus zu entwickeln ist f³nfmal h÷her (International Diabetes Federation).
Es gibt verschiedene Definitionen f³r das Metabolische Syndrom. Am hõufigsten wird f³r die Diagnose wohl die Definition des National Cholesterol Education Program (NCEP-ATP-III) verwendet. Danach m³ssen mindestens drei der unten angef³hrten Kriterien erf³llt sein (Grundy 2005):
Abdominelle (Bauch betreffende) Adipositas (Mõnner ≥ 102 cm Taillenumfang)
Erh÷hte Triglyzerid-Konzentration (≥ 150 mg/dl)
Erniedrigtes HDL-Cholesterin (Mõnner ≤ 40 mg/dl)
Erh÷hter Blutdruck (≥130/85 mmHg)
Erh÷hte N³chternglukose (≥ 110 mg/dl) (Blutabnahme vor dem Fr³hst³ck)
Durch die ADT werden diese Risikofaktoren f³r Herz-/Kreislauferkrankungen erh÷ht. Das oben erwõhnte, zusõtzliche Gewicht lagert sich als Fett vor allem im Bauchbereich an. Vielfach wurde auch wõhrend einer ADT ein erh÷hter Blutdruck festgestellt (Higano 2003)(Smith 2001a).
Mõnner, die eine ADT durchf³hren, entwickeln eine geringere Insulinempfindlichkeit und damit eine h÷here Insulinresistenz (Smith 2006) (Higano 2003). Es wird daher empfohlen, die ADT mit Metformin zu kombinieren (Nguyen 2015). Ob dies auch bei durch ADT induzierten Insulinresistenz zutrifft, ist umstritten (Mahalingam 2018). Die Frage, welche Wirkung die Einnahme von Metformin hat, um dieses Risiko zu reduzieren und gleichzeitig den Tumor zu bekõmpfen, wird derzeit im Rahmen der STAMPEDE Studie untersucht (Gilbert 2018).
Schlie▀lich wird auch der Fettstoffwechsel durch die ADT verõndert. So erh÷ht sich jeweils im Mittel der Cholesterinspiegel um 9 %, das High Density Lipoprotein Cholesterin, kurz HDL-C, um 11,3 % und das Low Density Lipoprotein Cholesterin, kurz LDL-C, um 7,3 %. Dar³ber hinaus erh÷hten sich die Triglyceride um 26,5 % (Higano 2003). Diese erh÷hten Blutwerte bzw. Fettstoffwechselst÷rungen sind Kennzeichen f³r ein metabolisches Syndrom. Es ist daher nachvollziehbar, dass in einer Studie bei ³ber 50% der Patienten wõhrend einer langfristigen ADT ein metabolisches Syndrom festgestellt wurde wõhrend dies nur bei 20% der gesunden Mõnner der Fall war (Braga-Basaria 2006). Es ist daher sinnvoll, Patienten vor einer ADT auf diese Risiken hinzuweisen, eine Ernõhrungsberatung durchzuf³hren und wõhrend der Therapie die Faktoren f³r ein metabolisches Syndrom zu ³berwachen (Mitzuzuka).
Es gibt Medikamente um einige der Symptome des metabolischen Syndroms zu lindern. So kann das Cholesterin mit Statinen gesenkt werden, es gibt blutdrucksenkende Mittel gegen Bluthochdruck und Thrombozytenaggregationshemmer, wie z.B. Aspirin, zur Verhinderung von Blutgerinnseln. Au▀erdem wurde in einer Studie festgestellt, dass eine Ergõnzung der ADT mit Toremifen den Cholesterinspiegel um 4,7% senkte, das LDL-C um 7,0% und Triglyceride um 17,6%. Dagegen stieg das HDL-C um 7,2% (Smith 2010). Ein zu niedriges HDL-C ist ein Risikofaktor. Sinnvoller ist allerdings eine gesunde Ernõhrung und sportliche Betõtigung. Die aus dem metabolischen Syndrom resultierenden kardiovaskulõren Risiken bei Patienten wõhrend einer ADT werden im folgenden Kapitel dargestellt.
8 Kardiovaskulõre Risiken und Diabetes
In wie weit die ADT ein Risikofaktor f³r kardiovaskulõre Erkrankungen ist, konnte in Studien nicht eindeutig belegt werden. Hier eine ▄bersicht ³ber die vorliegenden Studien:

In der Graphik (O'Farrell 2015) sind oben die randomisierten Studien aufgef³hrt (RCT) und darunter die retrospektiven und beobachtenden Studien, die generell eine niedrigere Evidenz als die randomisierten Studien haben. Wenn der blaue Punkt links oder auf der senkrechten Linie liegt, so konnte ein Risiko f³r kardiovaskulõre Erkrankungen nicht nachgewiesen werden. Dagegen wird von einem Risiko f³r kardiovaskulõre Erkrankungen berichtet, wenn der blaue Punkt rechts von der senkrechten Linie liegt. Die randomisierten Studien konnten ³berwiegend kein Risiko f³r kardiovaskulõre Erkrankungen feststellen, die beobachtenden Studien, also die mit der niedrigeren Evidenz, dagegen schon. O'Farrell hat alle diese Studien zusammengefasst und f³r Patienten unter ADT ein um 21% (HR 1,21) erh÷htes, kardiovaskulõres Risiko errechnet. Ein niedrigeres Risiko errechnete er f³r Antiandrogene wie Bicalutamid. Hier ergab sich ein um 13% vermindertes Risiko gegen³ber der Kontrollgruppe. Da sich auch bei Patienten mit Orchiektomie ein erh÷htes kardiovaskulõres Risiko zeigte, schlie▀t O'Farrell daraus, dass das abgesenkte Testosteron durch die damit verbundenen metabolischen Symptome zu dem erh÷hten kardiovaskulõren Risiken f³hrt. Bicalutamid wõre danach besser als Hormontherapie f³r Patienten mit bestehenden kardiovaskulõren Risiken geeignet. Die Ergebnisse der Studie von O'Farrell werden teilweise in Zweifel gezogen (Shore 2019). In Verbindung mit weiteren Studien sah sich jedoch die amerikanische FDA veranlasst, auf den Beipackzetteln der GnRH-Analoga eine Warnung vor kardiovaskulõren Risiken zu verlangen und die American Heart Association gab eine Information heraus, in der vor kardiovaskulõren Risiken wõhrend einer ADT gewarnt wird (Levine 2010).
Unter Herz-Kreislauf-Erkrankungen versteht man Herzinfarkt, Herzstillstand, Herzversagen, Schlaganfall, Herzmuskelst÷rungen, Angina pectoris, Herzrhythmusst÷rungen und Erkrankung der Herzkranzgefõ▀e (Haque 2017). Der Grund f³r diese vermuteten kardiovaskulõren Risiken konnte bisher nicht mit Sicherheit ermittelt werden. Man nimmt an, dass sich durch die GnRH Analoga die Ablagerungen (arteriosklerotische Plaques) in den Arterien l÷sen. Werden diese mit dem Blut in kleinere Gefõ▀e gesp³lt, k÷nnen sie diese verstopfen. Dies kann eine Herz-Kreislauf-Erkrankung ausl÷sen (Roe 2016). Besonders betroffen von diesem Risiko sind Patienten, die vor Beginn der ADT bereits Herz-Kreislauf-Erkrankungen hatten (Haque 2017). Dies ist offenbar die Mehrheit der Prostatakrebspatienten. In einer Studie wurde festgestellt, dass 51% der Patienten diese Vorerkrankungen hatten und zusõtzlich 9% Diabetiker waren (Daskivich 2013).
Dies ist in sofern relevant, da Prostatakrebspatienten mit kardiovaskulõren Vorerkrankungen generell ein h÷heres Risiko haben aus anderen Gr³nden als Prostatakrebs zu versterben. In einer Studie waren Patienten ohne Vorerkrankungen nur in 16% der Fõlle, dagegen Patienten mit kardiovaskulõren Vorerkrankungen in 49% der Fõlle innerhalb von 10 Jahren aus anderen Gr³nden als Prostatakrebs verstorben (Chamie 2001, Figure 1). Kardiovaskulõre Erkrankungen stellen also ein erhebliches Risiko zu versterben dar, auch ohne ADT.
Einige Studien berichten, dass eine Therapie mit dem GnRH-Antagonisten Degarelix(Firmagon«) ein geringeres Risiko f³r Herz-Kreislauf-Erkrankungen haben soll. In der Studie von Margel wurde dies bei Patienten gezeigt, bei denen vor Beginn der ADT Herz-Kreislauf-Erkrankungen aufgetreten waren (Margel 2019). Bei 33,3 % dieser Patienten mit kardiovaskulõren Vorerkrankungen, die mit einem GnRH Analogon behandelt wurden, traten Herz-Kreislauf-Erkrankungen auf, wõhrend dies nur bei 4,8 % dieser Patienten der Fall war, die mit Degarelix behandelt wurden. Sicherlich wõren bei Patienten, die vor der ADT keine bestehenden kardiovaskulõren Risiken hatten, insgesamt niedrigere Prozentwerte ermittelt worden. Es wird gerade eine gro▀e Studie mit dem Namen PRONOUNCE durchgef³hrt, die klõren soll, ob Degarelix bei Patienten mit kardiovaskulõren Vorerkrankungen wirklich zu weniger kardiovaskulõren Problemen f³hrt als ein GnRH Analogon (Slovin 2018).
Man sollte daher wõhrend einer ADT die Risikofaktoren f³r Herz-Kreislauf-Erkrankungen reduzieren. Die Bundeszentrale f³r gesundheitliche Aufklõrung nennt folgende Risikofaktoren:
Ģ Rauchen
Ģ Hohe Cholesterinwerte
Ģ Zuckerkrankheit (Altersdiabetes Typ II)
Ģ Bluthochdruck
Ģ ▄bergewicht
Ģ Ungesunde Ernõhrung
Ģ Bewegungsmangel
Ģ Psychosoziale Stressoren
Viele dieser Faktoren werden aber durch die ADT gef÷rdert, wie hohe Cholesterinwerte (Smith 2002), Risiko von Diabetes, Gewichtszunahme und damit einhergehend Bluthochdruck sowie Stress durch die Tumorerkrankung und -behandlung.
Die American Heart Association empfiehlt das ABCDE System, um kardiovaskulõre Risiken zu reduzieren (Bhatia 2016):
A) Awareness und Aspirin: Bewusstsein f³r kardiovaskulõre Risiken beim Patienten erreichen, prophylaktisch eine 75 bis 100 mg Tablette Aspirin pro Tag einnehmen.
B) Blutdruck: dieser sollte unter 140/90 mm Hg liegen. Zur Senkung des Blutdrucks sollen ACE-Hemmer, wie Captopril, Enalapril usw., verwendet werden.
C) Cholesterin und Cigaretten: zu hohe Cholesterin-Werte k÷nnen durch eine Diõt oder mit Statinen in den Referenzbereich gebracht werden. Das Rauchen sollte wegen der vielfõltigen, schõdlichen Wirkungen eingestellt werden.
D) Diabetes und Diõt: der Blutzucker-Wert sollte ³berwacht werden und durch Diõt oder Metformin eine Diabetes-Erkrankung vermieden werden. Die Ernõhrung sollte auf mehr Fr³chte, Gem³se und Vollwertbrot umgestellt werden. Mit der Nahrung sollten mehr als 600 IU Vitamin D und weniger als 1200 mg Kalzium pro Tag aufgenommen werden.
E) Exercise (Sport): 150 Minuten moderater Sport sollte in der Woche durchgef³hrt werden. Unge³bte Patienten sollten anfangs mit weniger Minuten beginnen.
Diabetes ist eine Gruppe von Stoffwechselst÷rungen des Kohlenhydratstoffwechsels. Sie entstehen durch einen Mangel an Insulin oder einer abgeschwõchten Wirksamkeit des Insulins (Insulinresistenz). Die daraus resultierende chronische ▄berzuckerung f³hrt zu Schõden am Nervensystem und am Blutgefõ▀system.
Die ADT steigert das K÷rperfett in der Bauchregion, das als Risikofaktor f³r Diabetes gilt. Au▀erdem reduziert sie innerhalb von zw÷lf Wochen die Insulinresistenz und damit ebenfalls das Risiko f³r Diabetes (Keating 2006). Einen Zusammenhang zwischen Diabetes und ADT belegt derzeit nur eine retrospektive Studie. Danach hatten Patienten mit einer ADT 42% hõufiger Diabetes als die Kontrollgruppe (Keating 2006).
9 Verkleinerung von Hoden und Penis
Eine lõngere ADT f³hrt zu einer Verkleinerung der Hoden auf etwa Haselnussgr÷▀e. Das ist bei 93% der Patienten der Fall (Walker 2013). Dies f³hrt zu bleiben Schõden, die auch die Produktion von Spermien erheblich schõdigen (Had×iselimović 1987). Die antihormonelle Therapie behindert die Bildung gesunder Spermien daher sehr stark und die Fruchtbarkeit geht normalerweise verloren.
Auch der Penis schrumpft (Higano 2003). In der Studie von Park wurde die eregierte Lõnge vor und nach der ADT gemessen. Vor der Therapie waren es im Mittel 10,76 cm. Nach 24 Monaten ADT war die Penislõnge im Mittel auf 8,05 cm zur³ckgegangen (Park 2011). Nach 15 Monaten ging die Lõnge nicht weiter zur³ck.
Grundsõtzlich vergr÷▀ern sich die Hoden und der Penis teilweise wieder, wenn die ADT beendet wird. Nach langer Dauer kann es aber sein, dass sich nur ein Hoden wieder erholt, was optisch zu einer asymetrischen Erscheinung f³hrt.
Meist wurden die Patienten vor einer ADT mit einer Prostataoperation oder Bestrahlung therapiert. Dies f³hrte ebenfalls zu einer Reduktion der Penislõnge. Die ADT reduziert die Penislõnge weiter.
1 Einleitung
2 Medikamente zur Durchf³hrung einer Hormontherapie
3 Wann ist eine Hormontherapie anzuwenden?
4 Hitzewallungen
5 Einschrõnkungen der Sexualitõt
6 Muskelschwund und Verringerung der physischen Leistungsfõhigkeit
7 Gewichtszunahme und metabolisches Syndrom
8 Kardiovaskulõre Risiken und Diabetes
9 Verkleinerung von Hoden und Penis
10 Brustwachstum/Gynõkomastie
11 Verlust der K÷rperbehaarung
12 Gelenkschmerzen
13 Knochenschwund und -br³che, Osteoporose
14 Blutarmut/Anõmie
15 Fatigue ¢ chronische M³digkeit
16 Psychische Beschwerden
17 Kognitive Verõnderungen
18 Trockene Augen
19 Erholung des Testosteronspiegels nach einer Hormontherapie
20 Hormontherapie mit Antiandrogenen
21 ųstrogene zur Linderung der Nebenwirkungen
22 Pharmakologie der Prõparate zur Hormontherapie
a) Zellbiologische Grundlagen
b) Orchiektomie
c) GnRH Analoga
d) GnRH Antagonisten
e) Antiandrogene
f) Hemmer der Testosteron-Biosynthese
g) Neue Androgenrezeptorhemmer
h) ųstrogene
23 Schlu▀betrachtung
24 Quellenverzeichnis
1 Einleitung
Die Hormontherapie ist eine sehr effektive Therapie gegen das Wachstum des Prostatakrebses. Fast alle Patienten, die nicht durch eine Operation oder Bestrahlung den Tumor beseitigen konnten, m³ssen irgendwann eine Hormontherapie machen. Diese Therapie wird dann f³r die verbleibende Lebenszeit angewendet. Oft wird auch bei einer Bestrahlung eine Hormontherapie von zwei bis drei Jahren durchgef³hrt.
Eine Hormontherapie ist mit vielen Nebenwirkungen verbunden. Diese treten nicht alle bei jedem Patienten auf und in der Regel auch mit individuell unterschiedlicher Intensitõt. An manche Nebenwirkungen gew÷hnen sich die Patienten auch und manche belasten dessen soziales Umfeld mehr als den Patienten selbst.
Der Arzt wird empfehlen, mit einer Hormontherapie zu beginnen, wenn er dies aus Sicht der Krebsbekõmpfung f³r richtig erachtet. Viele ─rzte sprechen mit dem Patienten nicht ³ber Nebenwirkungen. Sollte der Arzt ihm alle Nebenwirkungen eingehend erlõutern, w³rden die meisten Patienten gro▀e Bedenken haben mit einer Hormontherapie zu beginnen. Viele Patienten sprechen spõter die Nebenwirkungen beim Arzt nicht an oder wissen auch nicht, dass diese durch die Hormontherapie verursacht werden. Manche ─rzte bestõtigen dann nur, dass es sich um eine bekannte Nebenwirkung handelt. Der Arzt konzentriert sich auf die Wirkung der Hormontherapie, die durch die Entwicklung des PSA Wertes verfolgt wird und wird dem Patienten oft keine Empfehlungen geben, wie dieser mit den Nebenwirkungen umgehen kann. Entsprechend erwõhnt der Beipackzettel der eingesetzten Medikamente nur welche Nebenwirkungen auftreten k÷nnen, aber nicht, was der Patient dagegen tun k÷nnte. Da die Hormontherapie ³ber viele Jahre angewendet wird, kann dies zu einer gro▀e Belastung f³r den Patienten f³hren.
Wenn ein neues Medikament zugelassen werden soll, so bedarf dies gro▀er und teurer Studien, sogenannter Phase III Studien. In Bezug auf die Nebenwirkungen der Medikamente f³r eine Hormontherapie liegen keine entsprechenden, gro▀en Studien vor. Daher basieren die in dieser Arbeit verwendeten Studien auf kleineren Teilnehmerzahlen und haben daher nicht die hohe Evidenzkategorie wie gro▀e Phase III Studien. Dies muss man bei der Bewertung der Studienergebnisse ber³cksichtigen. Diese Studien liefern keine endg³ltigen Beweise, sind aber deutlich hilfreicher als keine Studien. Manchmal liegen auch Studien mit widersprechenden Ergebnissen vor. Im Rahmen dieser Arbeit konnte aber keine vergleichende Bewertung dieser Studien durchgef³hrt werden.
Es wird im folgenden ein ▄berblick ³ber die verschiedenen Nebenwirkungen gegeben, die bei einer Hormontherapie auftreten k÷nnen und die M÷glichkeiten zur Linderung oder Vermeidung dieser Nebenwirkungen aufgezeigt. Ziel ist es den betroffenen Patienten, die eine Hormontherapie machen m³ssen, damit zu helfen.
2 Medikamente zur Durchf³hrung einer Hormontherapie
Eine Hormontherapie kann mit verschiedenen Medikamenten durchgef³hrt werden. Fast immer sind dies sogenannte GnRH-Analoga (Leuprorelin, Goserelin, Triptorelin oder Buserelin) oder GnRH-Antagonisten (z.B. Degarelix). Au▀erdem k÷nnen die Hoden operativ entfernt werden, das ist die sogenannte Orchiektomie. Man bezeichnet die Hormontherapie auch als ADT, diese Abk³rzung steht f³r Androgendeprivationstherapie oder Androgenentzugstherapie. In dieser Arbeit wird die Androgenentzugstherapie mit GnRH-Analoga, GnRH-Antagonisten oder Orchiektomie als ADT bezeichnet und es werden die von diesen Mitteln verursachten Nebenwirkungen behandelt. Daneben gibt es noch Antiandrogene, vor allem Bicalutamid, die andere Nebenwirkungen zeigen und daher in einem gesonderten Kapitel behandelt werden. Die Therapie mit Antiandrogenen wird in diesem Text nicht als ADT bezeichnet. Wird dagegen von Hormontherapie gesprochen, so ist beides, eine ADT und eine Therapie mit Antiandrogenen gemeint.
Die Prostatakrebszellen besitzen Androgen-Rezeptoren die das Testosteron im K÷rper eines Mannes binden. Dieses Testosteron ben÷tigt die Tumorzelle f³r ihr weiteres Wachstum. Wenn man den Testosteronspiegel im K÷rper durch eine ADT senkt, so k÷nnen die Tumorzellen kein Testosteron aufnehmen und das Wachstum dieser Zellen wird gestoppt. Manche Zellen sterben dadurch auch ab. Andere Tumorzellen sind jedoch resistent und wachsen trotzdem weiter, auch ohne oder mit nur sehr wenig Testosteron.
Eine ADT wird heute weit ³berwiegend medikament÷s durchgef³hrt, das operative Entfernen der Hoden, die Orchiektomie, wird nur noch selten angewandt. Man kann diese Operation nicht mehr r³ckgõngig machen, wenn starke Nebenwirkungen auftreten sollten. Es sei denn, man f³hrt das Testosteron durch Medikamente wieder zu.
Am hõufigsten werden GnRH-Agonisten eingesetzt. Dies sind Spritzen, die es in Ein-, Drei oder Sechs-Monats-Depots gibt. Diese GnRH-Agonisten gibt es in verschiedenen Wirkstoffen, die unter verschiedenen Handelsnamen angeboten werden:
Leuprorelin (Enantone«, Trenantone«, Eligard«)
Goserelin (Zoladex«)
Triptorelin (Decapeptyl«, Pamorelin«)
Buserelin (Profact«, Metrelef«, Suprecor«, Suprefact«)
Am bekanntesten ist der Wirkstoff Leuprorelin. Davon enthõlt Eligard« doppelt so viel wie die anderen beiden Medikamente Enantone« und Trenantone«.
Daneben gibt es GnRH-Antagonisten, von denen derzeit nur Firmagon« mit dem Wirkstoff Degarelix eine praktische Bedeutung hat.
Die im folgenden betrachteten Nebenwirkungen werden durch Orchiektomie, GnRH-Analoga und GnRH-Antagonisten verursacht. Diese Mittel senken den Testosteronspiegel im K÷rper ab. Es gibt daneben auch Antiandrogene, die als Tabletten eingenommen werden und eine ganz andere Wirkungsweise haben, so dass diese Nebenwirkungen nicht oder in erheblich geringerem Umfang auftreten. Die ─rzte gehen allgemein davon aus, dass diese Antiandrogene keine so effektive Wirkung gegen den Tumor haben wie die erwõhnten GnRH-Agonisten und GnRH-Antagonisten.
3 Wann ist eine Hormontherapie anzuwenden?
Die Nebenwirkungen eine ADT lassen sich nat³rlich am einfachsten vermeiden, in dem keine Hormontherapie durchgef³hrt wird. Man sollte daher jeweils genau pr³fen, ob wirklich eine Hormontherapie in der aktuellen Situation erforderlich ist. Es gibt verschiedene Krankheitsituationen, in denen eine Hormontherapie eingesetzt wird. Diese sind:
a) Umfangreiche Metastasen werden bereits bei der Diagnose festgestellt
In diesem Fall gehen die Leitlinien davon aus, dass der Krankheitsverlauf durch eine Operation oder Bestrahlung nicht mehr kurativ behandelt werden kann und empfehlen mit einer Hormontherapie zu beginnen. Diese wird dann lebenslang fortgef³hrt. Neuere Studien zeigen allerdings, dass der Krankheitsverlauf auch in dieser Situation durch eine Operation oder Bestrahlung positiv beeinflusst werden kann (Choudhury 2019)(Parker 2018)(Knipper 2019). Auf die Hormontherapie kann in diesem Fall aber trotzdem nicht verzichtet werden.
b) Als begleitende Therapie bei einer Bestrahlung
Wenn sich der Patient, meist bei fortgeschrittenem Alter, f³r eine Strahlentherapie der Prostata entscheidet, so zeigen Studien, dass der Erfolg dieser Strahlentherapie deutlich verbessert wird, wenn gleichzeitig mit einer ADT begonnen wird. Teilweise wird damit auch schon vor der Bestrahlung begonnen. Umstritten ist, wie lange die ADT in diesem Fall durchzuf³hren ist. Die grundlegende Studie dazu (Bolla 2009) empfiehlt eine Dauer von 36 Monaten, also drei Jahre. In dieser Studie wurde auch festgestellt, dass sechs Monate ADT keine entsprechende Wirkung hatten. Eine ADT ³ber drei Jahre ist f³r einen Patienten eine erhebliche Belastung und manche der eingetretenen Nebenwirkungen, wie erektile Dysfunktion, bilden sich oft nach dem Ende der ADT nicht mehr zur³ck. Kritiker dieser Studie wenden ein, dass zum Zeitpunkt dieser Studie mit niedrigeren Strahlendosen als heute gearbeitet wurde und daher jetzt m÷glicherweise eine k³rzere Dauer der begleitenden ADT m÷glich sei. Es gibt jetzt eine neuere, Phase-III Studie (Nabid 2018), die feststellte, dass 18 Monate begleitende ADT die gleiche Wirkung wie eine ADT ³ber 36 Monate hat. Bei neueren Bestrahlungstechniken, die mit h÷heren Strahlendosen arbeiten wie die SBRT Bestrahlung, konnte kein Vorteil f³r eine begleitende ADT festgestellt werden. Auch bei der Brachytherapie zeigte sich ein lõngeres ▄berleben bei nur 6 Monaten ADT gegen³ber einer lõngeren ADT (Stone 2018).
c) Als begleitende Therapie bei einer Salvage-Bestrahlung
Wenn nach einer Prostata-Operation der PSA Wert ansteigt, so wird oft eine Bestrahlung der Prostata durchgef³hrt, um dort m÷glicherweise vorhandene Tumorreste zu beseitigen. In diesem Fall sehen die Leitlinien keine begleitende Hormontherapie vor. In Studien wurde jedoch eine begleitende ADT von sechs Monaten (Carrie 2019) oder eine Hormontherapie mit Bicalutamid von 24 Monaten (Shipley 2017) mit gutem Erfolg durchgef³hrt. Vor allem bei Patienten mit h÷herem Risiko kann daher eine entsprechende Hormontherapie sinnvoll sein. Die Studie von Shipley wurde vor kurzem neu ausgewertet (Spratt 2019). Dabei wurde deutlich, dass die begleitende Hormontherapie nur bei Patienten mit hohem Risiko einen Vorteil zeigte. Als Patienten mit hohem Risiko wurden Betroffene mit eine PSA Wert von gr÷▀er 1,5 ng/ml vor Beginn der Bestrahlung eingestuft.
d) Bei einem biochemischen Rezidiv
In vielen Fõllen steigt nach einer Bestrahlung oder einer Salvage-Bestrahlung nach Operation der PSA Wert wieder an. In der Regel ist der Betroffene und sein soziales Umfeld dar³ber sehr besorgt. Die ³berwiegende Mehrheit der Urologen wird daraufhin mit einer ADT beginnen. Der PSA Wert fõllt daraufhin stark, der Patient ist zufrieden und der Arzt ebenfalls. Die Frage ist allerdings, ob angesichts der Nebenwirkungen einer ADT dieses Vorgehen in dieser Situation sinnvoll ist. Vorliegende Studien konnten durch eine Senkung des PSA Wertes kein lõngeres ▄berleben nachweisen. Zwei kleinere Studien (Messing 2006)(Duchesne 2016, TOAD Studie) k÷nnen auf Grund viel zu niedriger Teilnehmerzahlen keine validen Aussagen dazu machen. So zeigte eine gemeinsame Auswertung der TOAD und der ELAAT Studien keinen Vorteil f³r einen fr³hen Beginn der ADT (Loblaw 2018). Die Leitlinien empfehlen daher, den Anstieg des PSA Wertes nicht mit einer ADT zu bekõmpfen. Diese Empfehlung der Leitline bleibt jedoch weitgehend unbeachtet. So wurde in einer deutschen Studie festgestellt, dass 70% der Patienten, die mit einer ADT begannen, noch keine Metastasen zeigten (Hupe 2018).
Die Leitlinie erwõhnt, man solle bei einem steigenden PSA Wert in dieser Situation mit einer Hormontherapie beginnen bei (Leitlinie Prostatakarzinom, Erlõuterung zu Punkt 6.16):
Ģ einer PSA-Verdopplungszeit < 3 Monate;
Ģ symptomatischer lokaler Progression;
Ģ nachgewiesener Fernmetastasierung.
Man geht wohl davon aus, dass bei einer PSA-Verdopplungszeit kleiner als drei Monaten von vorhandenen Metastasen auszugehen ist. Unter symptomatischer lokaler Progression ist das Auftreten von Schmerzen durch Metastasen gemeint, mit Fernmetastasierung Metastasen au▀erhalb des Beckenbereichs. Diese Metastasen sollten aber mit einem CT oder Knochenszintigramm festgestellt werden und nicht mit einem PSMA PET/CT, das viel fr³her als die von der Leitlinie zugrunde gelegten Studien Metastasen nachweisen kann.
Wenn der Betroffene von dem PSA Anstieg sehr beunruhigt ist, kann man auch eine intermittierende Hormontherapie mit Bicalutamid durchf³hren, um den PSA Wert zu senken. Dieses Mittel hat nur geringe Nebenwirkungen und kann im sechsmonatigen Wechsel eingesetzt werden. Wenn Bicalutamid keine Wirkung mehr hat, k÷nnen ein GnRH-Analogon oder andere Medikamente wie Flutamid eingesetzt werden.
e) Hormontherapie nach einer Operation
Bei anderen Tumorarten, z.B. Darmkrebs, wird nach der Operation eine Chemotherapie durchgef³hrt, um verbliebene Tumorzellen dadurch abzut÷ten. Damit vergleichbar kann man auch nach einer Prostata-Operation eine sechsmonatige ADT durchf³hren. Wie in einer gro▀en Studie gezeigt wurde, f³hrt dies auch bei Patienten mit hohem Risiko zu einem sehr guten Krankheitsverlauf ³ber zehn Jahre nach der Operation (Dorff 2011, Hussain 2018a).
4 Hitzewallungen
Die ADT senkt den Testosteronspiegel und in der Folge davon den ųstrogenspiegel. Das Senken des ųstrogenspiegels bewirkt beim Mann Hitzewallungen wie sie auch von Frauen in den Wechseljahren bekannt sind (Russell 2017)(Taylor 2016). Diese Hitzewallungen treten bei etwa 60% der Mõnner wõhrend einer ADT auf (Walker 2013). Sie f³hren zu Schwindel, Herzklopfen und ausgeprõgten Schlafst÷rungen. Allein diese an sich harmlose Nebenwirkung veranlasst einen gro▀en Teil der Patienten die ADT abzubrechen (Allan 2014).

(Bild aus Frydenberg 2019)
Das abgesenkte ųstrogen senkt den Temperatursollwert im prõoptischen Bereich des vorderen Hypothalamus (Allan 2014). Die ─nderungen der Temperatur der Haut wird von spezialisierten Nervenzellen registriert und an das R³ckenmark gemeldet. Die Signale werden von dort aus ins Stammhirn weitergeleitet, und zwar an die Nervenzellen in einer Stammhirnregion namens Nukleus parabrachialis. Dies aktiviert wiederum die erwõhnte prõoptische Region (Nakamura 2008). Wurde dort der Temperatursollwert durch den ųstrogenmangel gesenkt, so beginnt man zu schwitzen obwohl die Au▀entemperatur dies nicht erforderlich machen w³rde. Dieser Temperatursollwert ist nun individuell unterschiedlich stark gest÷rt, so dass die Patienten unterschiedlich starke Beschwerden haben.
Bei Patienten, die diese Zusammenhõnge kennen, l÷sen diese Beschwerden keine Besorgnis aus. Luftdurchlõssige Kleidung aus Baumwolle, niedrige Temperaturen im Schlafzimmer und die Vermeidung bekannter Faktoren, die eine Hitzewallung ausl÷sen k÷nnen, erm÷glichen den Patienten diese Beschwerden zu bewõltigen. Als solche Faktoren werden genannt: erh÷hte Umgebungstemperaturen, Stress, Angstzustõnde, scharfe Lebensmittel, Kaffee und Alkohol. Als Hausmittel gegen Hitzewallungen wird auch Salbeitee empfohlen (Janzer 2009). Als Alternative zu Salbeitee gibt es auch Tabletten mit Salbeiblõtter-Trockenextrakt, die unter dem Namen Sweatosan angebotenen werden.
Frauen und teilweise auch Mõnner verwenden pflanzliche Mittel gegen Hitzewallungen. Dies sind die Wirkstoffe der Traubensilberkerze, die unter dem Namen Remifen und Remifen plus angeboten werden. Au▀erdem sibirischer Rhabarber, der unter dem Namen femiLoges im Handel ist. Dar³ber hinaus gibt es diverse Kombinationsprõparate mit verschiedenen weiteren Pflanzenstoffen. Man bezeichnet diese teilweise als Phyto÷strogene, da sie eine strukturelle ─hnlichkeit mit den ųstrogenen besitzen. Diese ─hnlichkeit erm÷glicht offenbar eine Bindung an ųstrogenrezeptoren.
Es gibt weitere M÷glichkeiten, diese Hitzewallungen zu bekõmpfen. Bei Frauen wird eine ųstrogen-Ersatztherapie mit ųstradiol-Pflastern angeboten. Da die Hitzewallungen auch beim Mann durch einen niedrigen ųstrogenspiegel verursacht werden, wirken diese Pflaster auch bei Mõnnern (Gerber 2000).
Man kann auch Medikamente nehmen, die allerdings mit Nebenwirkungen verbunden sind. So k÷nnen Antidepressiva der SNRI oder SSRI Klassen wie Gabapentin(Neurontin«) und Venlafaxin(Effexor«) oder auch Clonidin eingesetzt werden (Barbieri 2013) (Laufer 1982) (Loprinzi 1994) (Loprinzi 2009) (Boekhout 2008). Au▀erdem lassen sich Cyproteronacetat(Androcur«) oder eine Spritze Medroxyprogesteronacetat(MPA) (Provesa«) gegen Hitzewallungen einsetzen (Irani 2009).
Die Prostatakrebsleitlinie erwõhnt zur Linderung von Hitzewallungen Cyproteronacetat ä in einer Dosierung von 50 mg 2 x 1 Tbl. oder 300 mg i.m. alle zwei Wochenō. Au▀erdem werden ųstrogene und Progesteron sowie Clonidin oder Antidepressiva erwõhnt. (Leitlinie Prostatakarzinom, Erlõuterung zu Punkt 6.16)
Schlie▀lich kann auch Akupunktur eingesetzt werden, um die Hitzewallungen zu reduzieren (Beer 2010)(Frisk 2014). Damit konnten bei 41% der Patienten die Hitzewallungen um mehr als 50 % reduziert werden (Beer 2010). Empfohlen wird eine Behandlung zweimal die Woche wõhrend der ersten vier Wochen, danach einmal die Woche f³r sechs weitere Wochen. Folgende Punkte sollen dabei genadelt werden:
bilateral: Gallenblasen Gb 34, Blasen Bl 15, Bl 23, Bl 32,
unilateral: Dumai GV/Du 20, Herz He 7, Kreislauf Ks 6, Leber Le 2 und Milz Mi 6.
Die Punkte Bl 23 und Bl 32 erhalten eine Niedrig-Frequenz Elektrostimulation (2 Hz)
(Beer 2010). Die angegebenen Organe beziehen sich auf die Mediane, auf denen die Punkte liegen.
Bei all diesen Mitteln muss man ber³cksichtigen, dass ein Placebo bei etwa 25% der Patienten zu einer Besserung der Hitzewallungen um ³ber 50% f³hrt (Kaplan 2014). Dies entsprach in einer Studie der Wirkung von niedrig dosiertem Gabapentin (Loprinzi 2009).
5 Einschrõnkungen der Sexualitõt
Durch die ADT kommt es bei fast allen Patienten zu Erektionsst÷rungen, also einer erektilen Dysfunktion. Das hei▀t, es ist keine Erektion des Penis mehr m÷glich.

(Bild aus van Oort 2019)
Vielfach ist zusõtzlich die Potenz der Patienten bereits vor Beginn der ADT altersbedingt oder durch eine Operation oder Bestrahlung geschwõcht. Ebenfalls schwõcht die Gewichtszunahme wõhrend einer ADT die Potenz (Hatzimouratidis 2007). Dar³ber hinaus lõsst die Libido, also das Interesse an Sexualitõt, durch die ADT stark nach. Diese Nebenwirkungen m³ssen auch mit der Partnerin des Patienten besprochen werden, da die Partnerschaft davon sehr beeintrõchtigt werden kann. ▄ber 80% der Patienten stellen ihre sexuellen Aktivitõten wõhrend einer ADT ein (Walker 2013).
Jeder Mann hat nachts, meist unbemerkt, Erektionen. Diese finden nach Beginn der ADT auf Grund der Absenkung des Testosterons nicht mehr statt. Durch die mangelnde Libido reduziert der Patient ebenfalls die Zahl der Erektionen. Dies f³hrt nach ungefõhr sechs Monaten zu einer Penisatropie, die Schwellk÷rper schrumpfen und eine Erektion ist nicht mehr m÷glich, da das Abflie▀en des Blutes aus den Schwellk÷rpern nicht mehr verhindert werden kann (Aoun 2015). Diese Penisatropie beginnt sich schon nach einigen Wochen zu entwickeln. Daher sind ein gro▀er Teil der Patienten auch nach dem Ende der ADT dauerhaft impotent. Dem kann nur entgegengewirkt werden, wenn der Patient trotz mangelnder Libido regelmõ▀ig f³r Erektionen sorgt! Eine Impotenz nach dem Ende der ADT wird in vielen Fõllen die Partnerschaft weiter belasten. Sie hat oft gravierende Auswirkungen auf die Psyche. Es kann zur Vereinsamung aufgrund von Scham, auf eine Einstellung sexueller Aktivitõten und einem Verlust des Selbstwertgef³hls kommen.
Ein Mann kann auch ohne Erektion durch entsprechende Stimulation einen Orgasmus haben. Auch die Frau ben÷tigt keine Penetration, um zu einem Orgasmus zu kommen. Viele Paare haben daher gemeinsamen Sex in dem sie sich entsprechend darauf eingestellt haben. Dar³ber hinaus lõsst sich eine erektile Dysfunktion durch Medikamente, die die Erektion verstõrken oder andere Ma▀nahmen teilweise beheben. Geeignete Medikamente sind z.B. Sildenafil (Viagra«) oder Tadalafil (Cialis«), die mittlerweile als Generika verf³gbar sind. Der Testosteron-Entzug wõhrend einer ADT soll allerdings die Wirkung dieser Medikamente reduzieren (White 2015) (Alhathal 2012). Dies gilt insbesondere wenn bereits eine Penisatropie eingetreten ist.
Alternativ gibt es auch den Wirkstoff Alprostadil, der vom Patienten selbst injiziert werden muss. Dieser ist auch dann wirksam, wenn die Erektionsst÷rungen durch eine Schõdigung der Nerven im Rahmen einer Prostataoperation hervorgerufen wurden. Dieser Wirkstoff kann als Fertigspritze, Harnr÷hrenstõbchen (MUSE«) oder Gel verabreicht werden. Die Spritze hat etwa die Gr÷▀e einer Insulinspritze und damit wird das Mittel direkt in den Schwellk÷rper des Penis injiziert. Man nennt dies auch eine Schwellk÷rper-Autoinjektions-Therapie (SKAT). Das Gel wird dagegen mit einem Applikator in die Harnr÷hre gedr³ckt. Die erste Anwendung und Einweisung erfolgt in der Regel durch den Urologen, der erst danach ein Rezept ausstellen sollte.
Eine Erektion lõsst sich auch mit einer Vakuumpumpe herbeif³hren. Anschlie▀end wird ein Gummiring ³ber die Penisbasis gest³lpt, der das Abflie▀en des Blutes verhindert. Nach einiger ▄bung ist das erfolgreich einsetzbar.
Schlie▀lich gibt es noch Schwellk÷rperprothesen, die im Rahmen einer Operation in den Penis implantiert werden. Diese Operation kann recht schmerzhaft sein. Alle diese Mittel setzen allerdings voraus, dass trotz ADT ausreichend Libido f³r sexuelle Aktivitõten verblieben ist.
6 Muskelschwund und Verringerung der physischen Leistungsfõhigkeit
Durch das Absenken des Testosteronspiegels kommt es zu einer Reduktion der Muskelmasse (Sarkopenie). Nach 12 Monaten sind beispielsweise einer Studie von Smith zufolge im Mittel 3,8 % der Muskelmasse zur³ckgegangen (Smith 2004). Dies f³hrt zu einer verminderten Leistungsfõhigkeit, die sich bei den Patienten meist deutlich bemerkbar macht (Storer 2012). Treppensteigen, bergauf gehen usw. fõllt deutlich schwerer. Im Bodybuilding Bereich wird oft Testosteron zugef³hrt, um die Muskelmasse zu erh÷hen. Entsprechend vermindert sich die Muskelmasse, wenn das Testosteron durch eine ADT gesenkt wird.
Dem Muskelschwund kann nur durch regelmõ▀iges Krafttraining entgegengewirkt werden (GalvŃo 2006). Frauen, k÷nnen trotz niedrigem Testosteronspiegel durch Krafttraining Muskeln aufbauen. Krafttraining bedeutet Gewichtheben, Kniebeugen, Klimmz³ge, Liegest³tzen oder ▄bungen an entsprechenden Gerõten, die am besten in einem Fitnesszentrum unter Anleitung eines Trainers durchgef³hrt werden. Krafttraining verbessert das Befinden der Patienten deutlich (Segal 2003).
7 Gewichtszunahme und metabolisches Syndrom
Nach dem Beginn der ADT tritt bei den meisten Patienten eine Gewichtszunahme ein. Diese ist nicht durch die Testosteronabsenkung sondern durch die resultierende ųstrogenabsenkung bedingt (Finkelstein 2013).

(Bild aus Meerleer 2016)
Die Gewichtszunahme betrõgt im Mittel 1,8%, dies sind bei einem Gewicht von 90 kg also 1,6 kg. Wie bereits erwõhnt, geht jedoch die Muskelmasse zur³ck (sarcopenic obesity). Der dadurch bedingte Gewichtsverlust wird durch einen Zuwachs an K÷rperfett ³berkompensiert. Das K÷rperfett erh÷ht sich um 11%, also ganz erheblich (Smith 2004). Andere Studien berichten von unterschiedlichen Werten. Der Zuwachs an K÷rperfett erh÷ht die kardiovaskulõren Risiken und kann zu einem metabolischen Syndrom f³hren (Smith 2001a). Die Symptome f³r ein metabolische Syndrom beginnen sich bereits innerhalb von 12 bis 24 Wochen nach Beginn der ADT zu entwickeln (žstergren 2018)(Mitzuzuka 2016).
Unter dem Begriff äMetabolisches Syndromō werden verschiedene Krankheiten und Risikofaktoren f³r Herz-/Kreislauferkrankungen zusammengefasst, die sich in der Regel durch eine ▄berernõhrung entwickeln. Folgende Symptome bzw. Krankheitsbilder treten beim Metabolischen Syndrom meist gemeinsam auf (Nguyen 2015):
Ģ starkes ▄bergewicht mit meist bauchbetonter Fetteinlagerung (Adipositas)
Ģ Bluthochdruck
Ģ erh÷hter Blutzuckerspiegel (gest÷rter Zuckerstoffwechsel in Form einer
Ģ Insulinunempfindlichkeit bzw. -Resistenz), eine Hauptursache f³r Diabetes
Ģ gest÷rter Fettstoffwechsel, Hypertriglyzeridõmie und erniedrigtes HDL-Cholesterin
Das metabolische Syndrom wird neben dem Rauchen als der entscheidende Risikofaktor f³r Erkrankungen der arteriellen Gefõ▀e, insbesondere die koronare Herzkrankheit, angesehen. Mõnner mit einem metabolischen Syndrom sterben doppelt so hõufig an einem Herzinfarkt oder Schlaganfall wie gesunde Mõnner. Das Risiko eine Diabetes mellitus zu entwickeln ist f³nfmal h÷her (International Diabetes Federation).
Es gibt verschiedene Definitionen f³r das Metabolische Syndrom. Am hõufigsten wird f³r die Diagnose wohl die Definition des National Cholesterol Education Program (NCEP-ATP-III) verwendet. Danach m³ssen mindestens drei der unten angef³hrten Kriterien erf³llt sein (Grundy 2005):
Abdominelle (Bauch betreffende) Adipositas (Mõnner ≥ 102 cm Taillenumfang)
Erh÷hte Triglyzerid-Konzentration (≥ 150 mg/dl)
Erniedrigtes HDL-Cholesterin (Mõnner ≤ 40 mg/dl)
Erh÷hter Blutdruck (≥130/85 mmHg)
Erh÷hte N³chternglukose (≥ 110 mg/dl) (Blutabnahme vor dem Fr³hst³ck)
Durch die ADT werden diese Risikofaktoren f³r Herz-/Kreislauferkrankungen erh÷ht. Das oben erwõhnte, zusõtzliche Gewicht lagert sich als Fett vor allem im Bauchbereich an. Vielfach wurde auch wõhrend einer ADT ein erh÷hter Blutdruck festgestellt (Higano 2003)(Smith 2001a).
Mõnner, die eine ADT durchf³hren, entwickeln eine geringere Insulinempfindlichkeit und damit eine h÷here Insulinresistenz (Smith 2006) (Higano 2003). Es wird daher empfohlen, die ADT mit Metformin zu kombinieren (Nguyen 2015). Ob dies auch bei durch ADT induzierten Insulinresistenz zutrifft, ist umstritten (Mahalingam 2018). Die Frage, welche Wirkung die Einnahme von Metformin hat, um dieses Risiko zu reduzieren und gleichzeitig den Tumor zu bekõmpfen, wird derzeit im Rahmen der STAMPEDE Studie untersucht (Gilbert 2018).
Schlie▀lich wird auch der Fettstoffwechsel durch die ADT verõndert. So erh÷ht sich jeweils im Mittel der Cholesterinspiegel um 9 %, das High Density Lipoprotein Cholesterin, kurz HDL-C, um 11,3 % und das Low Density Lipoprotein Cholesterin, kurz LDL-C, um 7,3 %. Dar³ber hinaus erh÷hten sich die Triglyceride um 26,5 % (Higano 2003). Diese erh÷hten Blutwerte bzw. Fettstoffwechselst÷rungen sind Kennzeichen f³r ein metabolisches Syndrom. Es ist daher nachvollziehbar, dass in einer Studie bei ³ber 50% der Patienten wõhrend einer langfristigen ADT ein metabolisches Syndrom festgestellt wurde wõhrend dies nur bei 20% der gesunden Mõnner der Fall war (Braga-Basaria 2006). Es ist daher sinnvoll, Patienten vor einer ADT auf diese Risiken hinzuweisen, eine Ernõhrungsberatung durchzuf³hren und wõhrend der Therapie die Faktoren f³r ein metabolisches Syndrom zu ³berwachen (Mitzuzuka).
Es gibt Medikamente um einige der Symptome des metabolischen Syndroms zu lindern. So kann das Cholesterin mit Statinen gesenkt werden, es gibt blutdrucksenkende Mittel gegen Bluthochdruck und Thrombozytenaggregationshemmer, wie z.B. Aspirin, zur Verhinderung von Blutgerinnseln. Au▀erdem wurde in einer Studie festgestellt, dass eine Ergõnzung der ADT mit Toremifen den Cholesterinspiegel um 4,7% senkte, das LDL-C um 7,0% und Triglyceride um 17,6%. Dagegen stieg das HDL-C um 7,2% (Smith 2010). Ein zu niedriges HDL-C ist ein Risikofaktor. Sinnvoller ist allerdings eine gesunde Ernõhrung und sportliche Betõtigung. Die aus dem metabolischen Syndrom resultierenden kardiovaskulõren Risiken bei Patienten wõhrend einer ADT werden im folgenden Kapitel dargestellt.
8 Kardiovaskulõre Risiken und Diabetes
In wie weit die ADT ein Risikofaktor f³r kardiovaskulõre Erkrankungen ist, konnte in Studien nicht eindeutig belegt werden. Hier eine ▄bersicht ³ber die vorliegenden Studien:

In der Graphik (O'Farrell 2015) sind oben die randomisierten Studien aufgef³hrt (RCT) und darunter die retrospektiven und beobachtenden Studien, die generell eine niedrigere Evidenz als die randomisierten Studien haben. Wenn der blaue Punkt links oder auf der senkrechten Linie liegt, so konnte ein Risiko f³r kardiovaskulõre Erkrankungen nicht nachgewiesen werden. Dagegen wird von einem Risiko f³r kardiovaskulõre Erkrankungen berichtet, wenn der blaue Punkt rechts von der senkrechten Linie liegt. Die randomisierten Studien konnten ³berwiegend kein Risiko f³r kardiovaskulõre Erkrankungen feststellen, die beobachtenden Studien, also die mit der niedrigeren Evidenz, dagegen schon. O'Farrell hat alle diese Studien zusammengefasst und f³r Patienten unter ADT ein um 21% (HR 1,21) erh÷htes, kardiovaskulõres Risiko errechnet. Ein niedrigeres Risiko errechnete er f³r Antiandrogene wie Bicalutamid. Hier ergab sich ein um 13% vermindertes Risiko gegen³ber der Kontrollgruppe. Da sich auch bei Patienten mit Orchiektomie ein erh÷htes kardiovaskulõres Risiko zeigte, schlie▀t O'Farrell daraus, dass das abgesenkte Testosteron durch die damit verbundenen metabolischen Symptome zu dem erh÷hten kardiovaskulõren Risiken f³hrt. Bicalutamid wõre danach besser als Hormontherapie f³r Patienten mit bestehenden kardiovaskulõren Risiken geeignet. Die Ergebnisse der Studie von O'Farrell werden teilweise in Zweifel gezogen (Shore 2019). In Verbindung mit weiteren Studien sah sich jedoch die amerikanische FDA veranlasst, auf den Beipackzetteln der GnRH-Analoga eine Warnung vor kardiovaskulõren Risiken zu verlangen und die American Heart Association gab eine Information heraus, in der vor kardiovaskulõren Risiken wõhrend einer ADT gewarnt wird (Levine 2010).
Unter Herz-Kreislauf-Erkrankungen versteht man Herzinfarkt, Herzstillstand, Herzversagen, Schlaganfall, Herzmuskelst÷rungen, Angina pectoris, Herzrhythmusst÷rungen und Erkrankung der Herzkranzgefõ▀e (Haque 2017). Der Grund f³r diese vermuteten kardiovaskulõren Risiken konnte bisher nicht mit Sicherheit ermittelt werden. Man nimmt an, dass sich durch die GnRH Analoga die Ablagerungen (arteriosklerotische Plaques) in den Arterien l÷sen. Werden diese mit dem Blut in kleinere Gefõ▀e gesp³lt, k÷nnen sie diese verstopfen. Dies kann eine Herz-Kreislauf-Erkrankung ausl÷sen (Roe 2016). Besonders betroffen von diesem Risiko sind Patienten, die vor Beginn der ADT bereits Herz-Kreislauf-Erkrankungen hatten (Haque 2017). Dies ist offenbar die Mehrheit der Prostatakrebspatienten. In einer Studie wurde festgestellt, dass 51% der Patienten diese Vorerkrankungen hatten und zusõtzlich 9% Diabetiker waren (Daskivich 2013).
Dies ist in sofern relevant, da Prostatakrebspatienten mit kardiovaskulõren Vorerkrankungen generell ein h÷heres Risiko haben aus anderen Gr³nden als Prostatakrebs zu versterben. In einer Studie waren Patienten ohne Vorerkrankungen nur in 16% der Fõlle, dagegen Patienten mit kardiovaskulõren Vorerkrankungen in 49% der Fõlle innerhalb von 10 Jahren aus anderen Gr³nden als Prostatakrebs verstorben (Chamie 2001, Figure 1). Kardiovaskulõre Erkrankungen stellen also ein erhebliches Risiko zu versterben dar, auch ohne ADT.
Einige Studien berichten, dass eine Therapie mit dem GnRH-Antagonisten Degarelix(Firmagon«) ein geringeres Risiko f³r Herz-Kreislauf-Erkrankungen haben soll. In der Studie von Margel wurde dies bei Patienten gezeigt, bei denen vor Beginn der ADT Herz-Kreislauf-Erkrankungen aufgetreten waren (Margel 2019). Bei 33,3 % dieser Patienten mit kardiovaskulõren Vorerkrankungen, die mit einem GnRH Analogon behandelt wurden, traten Herz-Kreislauf-Erkrankungen auf, wõhrend dies nur bei 4,8 % dieser Patienten der Fall war, die mit Degarelix behandelt wurden. Sicherlich wõren bei Patienten, die vor der ADT keine bestehenden kardiovaskulõren Risiken hatten, insgesamt niedrigere Prozentwerte ermittelt worden. Es wird gerade eine gro▀e Studie mit dem Namen PRONOUNCE durchgef³hrt, die klõren soll, ob Degarelix bei Patienten mit kardiovaskulõren Vorerkrankungen wirklich zu weniger kardiovaskulõren Problemen f³hrt als ein GnRH Analogon (Slovin 2018).
Man sollte daher wõhrend einer ADT die Risikofaktoren f³r Herz-Kreislauf-Erkrankungen reduzieren. Die Bundeszentrale f³r gesundheitliche Aufklõrung nennt folgende Risikofaktoren:
Ģ Rauchen
Ģ Hohe Cholesterinwerte
Ģ Zuckerkrankheit (Altersdiabetes Typ II)
Ģ Bluthochdruck
Ģ ▄bergewicht
Ģ Ungesunde Ernõhrung
Ģ Bewegungsmangel
Ģ Psychosoziale Stressoren
Viele dieser Faktoren werden aber durch die ADT gef÷rdert, wie hohe Cholesterinwerte (Smith 2002), Risiko von Diabetes, Gewichtszunahme und damit einhergehend Bluthochdruck sowie Stress durch die Tumorerkrankung und -behandlung.
Die American Heart Association empfiehlt das ABCDE System, um kardiovaskulõre Risiken zu reduzieren (Bhatia 2016):
A) Awareness und Aspirin: Bewusstsein f³r kardiovaskulõre Risiken beim Patienten erreichen, prophylaktisch eine 75 bis 100 mg Tablette Aspirin pro Tag einnehmen.
B) Blutdruck: dieser sollte unter 140/90 mm Hg liegen. Zur Senkung des Blutdrucks sollen ACE-Hemmer, wie Captopril, Enalapril usw., verwendet werden.
C) Cholesterin und Cigaretten: zu hohe Cholesterin-Werte k÷nnen durch eine Diõt oder mit Statinen in den Referenzbereich gebracht werden. Das Rauchen sollte wegen der vielfõltigen, schõdlichen Wirkungen eingestellt werden.
D) Diabetes und Diõt: der Blutzucker-Wert sollte ³berwacht werden und durch Diõt oder Metformin eine Diabetes-Erkrankung vermieden werden. Die Ernõhrung sollte auf mehr Fr³chte, Gem³se und Vollwertbrot umgestellt werden. Mit der Nahrung sollten mehr als 600 IU Vitamin D und weniger als 1200 mg Kalzium pro Tag aufgenommen werden.
E) Exercise (Sport): 150 Minuten moderater Sport sollte in der Woche durchgef³hrt werden. Unge³bte Patienten sollten anfangs mit weniger Minuten beginnen.
Diabetes ist eine Gruppe von Stoffwechselst÷rungen des Kohlenhydratstoffwechsels. Sie entstehen durch einen Mangel an Insulin oder einer abgeschwõchten Wirksamkeit des Insulins (Insulinresistenz). Die daraus resultierende chronische ▄berzuckerung f³hrt zu Schõden am Nervensystem und am Blutgefõ▀system.
Die ADT steigert das K÷rperfett in der Bauchregion, das als Risikofaktor f³r Diabetes gilt. Au▀erdem reduziert sie innerhalb von zw÷lf Wochen die Insulinresistenz und damit ebenfalls das Risiko f³r Diabetes (Keating 2006). Einen Zusammenhang zwischen Diabetes und ADT belegt derzeit nur eine retrospektive Studie. Danach hatten Patienten mit einer ADT 42% hõufiger Diabetes als die Kontrollgruppe (Keating 2006).
9 Verkleinerung von Hoden und Penis
Eine lõngere ADT f³hrt zu einer Verkleinerung der Hoden auf etwa Haselnussgr÷▀e. Das ist bei 93% der Patienten der Fall (Walker 2013). Dies f³hrt zu bleiben Schõden, die auch die Produktion von Spermien erheblich schõdigen (Had×iselimović 1987). Die antihormonelle Therapie behindert die Bildung gesunder Spermien daher sehr stark und die Fruchtbarkeit geht normalerweise verloren.
Auch der Penis schrumpft (Higano 2003). In der Studie von Park wurde die eregierte Lõnge vor und nach der ADT gemessen. Vor der Therapie waren es im Mittel 10,76 cm. Nach 24 Monaten ADT war die Penislõnge im Mittel auf 8,05 cm zur³ckgegangen (Park 2011). Nach 15 Monaten ging die Lõnge nicht weiter zur³ck.
Grundsõtzlich vergr÷▀ern sich die Hoden und der Penis teilweise wieder, wenn die ADT beendet wird. Nach langer Dauer kann es aber sein, dass sich nur ein Hoden wieder erholt, was optisch zu einer asymetrischen Erscheinung f³hrt.
Meist wurden die Patienten vor einer ADT mit einer Prostataoperation oder Bestrahlung therapiert. Dies f³hrte ebenfalls zu einer Reduktion der Penislõnge. Die ADT reduziert die Penislõnge weiter.




























.png)














Kommentar